
全例調査Q&A改正のポイント専門家の視点 -RWDの現場から-
2026.01.30
2026.01.28
全例調査Q&A改正が示す「調査の位置づけ」の変化
ディシジョンツリー改正と同じく、鍵は「科学的根拠」
医療用医薬品の全例調査方式による使用成績調査に関するQ&A」の一部改正が令和6年7月18日、厚生労働省医薬局医薬品審査管理課から通知されました。今回の改正は、全例調査の手順を細かく変えるというより、「全例調査をどう位置づけ、どう説明するか」を、ディシジョンツリー改正の考え方に沿って整理した点に特徴があります。
「全例調査=とりあえず実施」から、「目的に照らして選択」へ
改正後のQ1では、承認条件としての全例調査を、一定症例数が集積されるまで使用患者の背景情報や安全性/有効性情報を可能な限り偏りなく収集し、承認内容の再確認や適正使用に必要な情報を収集する手段として整理しています。
言い換えると、全例調査は「承認条件だから“自動的に”採る」のではなく、確認したい事項に対して適した情報収集の方法として選択するという整理です。これは、目的から調査を組み立てるというディシジョンツリー改正の考え方と同じ流れです。
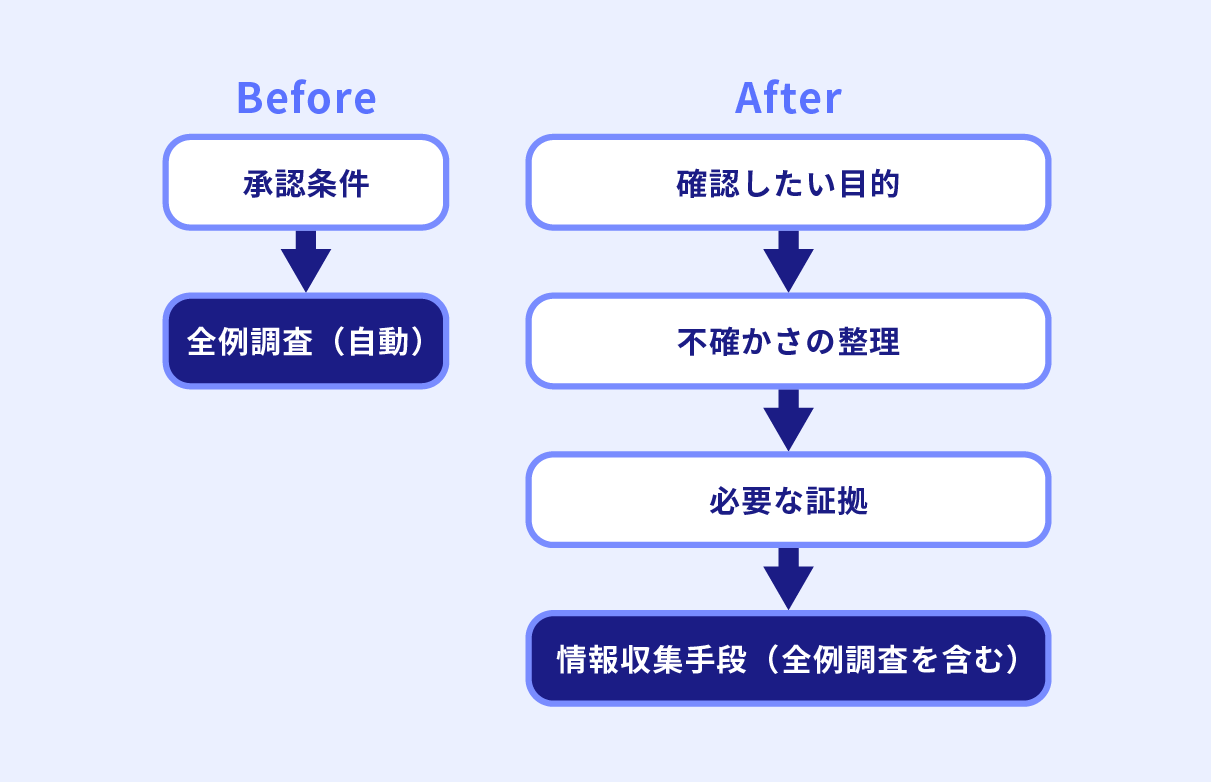
2) 変化点1:日本人治験症例が少ない「だけ」では、原則として全例調査は選ばない
もどる

© Medical Data Vision Co., Ltd. All Rights Reserved.




